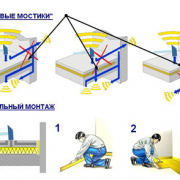
Виды и способы удаления коррозии металла
Содержание:
- Причины появления коррозии
- Как обеспечить протекторную защиту
- Методы защиты от коррозии металла
- 2 Защита от коррозии посредством специальных покрытий
- 2 Антикоррозионная защита при помощи протекторов – особенности методики
- 1 Суть протекторной защиты металлов от коррозии
- Как отчистить ржавчину с кузова автомобиля
- Применение жидкой резины для гидроизоляционных работ
- Виды коррозии металлов
- Оцинковка кузова
- Происхождение термина «Холодное цинкование»
- Защитные покрытия, применяемые в быту.
Причины появления коррозии
Развитие коррозии трубопроводов происходит в результате реакции окисления металла от постоянного воздействия влажной среды. Изменяется состав металла на ионном уровне. На данный процесс может оказывать влияние состав жидкости, протекающей внутри трубопровода. Причины возникновения ржавчины могут быть следующими:
- Сплавы, из которых изготовлены трубопроводы, имеют различные электрохимические потенциалы. Это вызывает протекание токов по трубе. Разные потенциалы могут возникать вследствие изменений составляющих грунта, а также разными параметрами показателей окружающей среды.
- Грунтовые воды или влага, находящаяся в почве.
- Химический состав почвы, в том числе наличие кислотных примесей во внешней среде.
- Состав транспортируемой трубопроводом жидкости.
- Наличие в грунте блуждающих токов.
Это интересно: 40 способов необычного применения WD-40 — познавайте с нами
Как обеспечить протекторную защиту
Покрытие труб специальными составами — это задача не только производителя, в процессе эксплуатации конструкции обеспечение защитных свойств тоже должно выполняться. Всего существует несколько способов защиты металла от воздействия агрессивных сред:
- химическая обработка;
- покрытие стенок специальными составами;
- защита от блуждающих токов;
- подведение катода или анода.
О пассивных и активных способах
Антикоррозионная защита — это целый комплекс мероприятий, проводимых предприятиями. Пассивные методы защиты предполагают выполнение следующих работ:
- На стадии монтажа между трубопроводом и грунтом оставляют воздушный зазор, препятствующий попаданию грунтовой воды, в том числе в составе с кислотными и щелочными примесями.
- Покрытие специализированными составами, назначение которых распространяется от негативных воздействий почвы.
- Обработка металла химическими составами, с образованием тонкой пленки.
Активные способы защиты предусматривают использование тока и обмен ионов на основе химических реакций, за счет чего обеспечивается:
- Защита подземных трубопроводов от коррозии созданием электродренажной системы для изоляции трубопроводного транспорта от блуждающих токов.
- Защита анодом от разрушения металлических поверхностей.
- Катодная защита для увеличения сопротивления металлических оснований.
Только с учетом всех способов, препятствующих образованию ржавчины на металле, будет увеличен срок службы конструкций. Антикоррозионная защита трубопроводов должна выполняться комплексно.
На видео: защита трубопроводов и кабельных линий от электрической коррозии.
https://youtube.com/watch?v=l_pU59HIdlo
О достоинствах применения протекторов
Защита труб этим способом производится с добавлением компонента — ингибитора. Это материал с отрицательным электрическим зарядом. Под воздействием воздушных масс он растворяется, а конструкция остается целой и не подвергается ржавлению. Протекторная защита от коррозии применяется для продления срока службы строительных конструкций, систем отопления и водоснабжения, а также магистрального и промыслового трубопроводного транспорта.
Применение электрохимической защиты позволяет устранить причины многих видов коррозии. Такая антикоррозийная защита трубопроводов – неплохое решение даже для предприятий, не имеющих финансовых возможностей по обеспечению полноценной защиты от неконтролируемого процесса.
Для обеспечения грамотного подхода следует:
- Протекторы, изготовленные из алюминия, использовать в средах морских вод и прибрежных шельфах.
- В средах с небольшой электропроводностью использовать магниевые протекторы. Но, опять же, они не подходят для обработки внутреннего покрытия резервуаров, нефтяных отстойников в связи с тем, что обладают достаточно низкой взрывопожароопасностью.
- Использовать протекторы для защиты от сред пресной воды.
- Проекторы, выполненные на основе цинка, являются полностью безопасными, их можно применять на пожаро- и взрывоопасных производствах.
Протекторной антикоррозионной защите можно отнести следующий ряд преимуществ:
- недостаток денежных средств и производственных мощностей у предприятия не будет препятствием ее выполнению;
- возможность защиты конструкций небольших размеров;
- если трубы покрыты теплоизоляционными материалами, то такая защита приемлема.
Используемые материалы и цели применения
Противокоррозионная защита необходима для всех металлических оснований. Данный вид противостояния от ржавчины широко используется для обработки танкеров, так как эти суда наиболее подвержены воздействию воды, имеющей в составе агрессивные компоненты. Даже специальная окраска не справляется с решением этой проблемы.
Наиболее рациональным выбором для покрытия стальных конструкций будет использование протекторов с отрицательным потенциалом. При изготовлении таких устройств применяется магний, цинк или алюминий. Большая разница потенциалов металла и стальных поверхностей способствует увеличению спектра защитного действия, в результате различные виды коррозии устраняются.
Пассивная защита требуется стальным покрытиям и изделиям из металла. Сущность метода заключается в применении гальванических анодов, обеспечивающих противодействие подземных трубопроводов коррозии. При произведении расчета для данной установки, необходимо учитывать следующие показатели:
- параметры силы тока;
- сопротивление от перепадов напряжения;
- характеристики степени защиты, применяемые для 1 км трубопровода;
- показатель расстояния между элементами защиты.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия.
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях. Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием. Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия.
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия.
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
2 Защита от коррозии посредством специальных покрытий
Чтобы защитное покрытие справлялось с задачами, которые возлагаются на него, оно должно обладать целым рядом особых качеств:
- быть износостойким и максимально твердым;
- характеризоваться высоким показателем прочности сцепления с поверхностью обрабатываемого изделия (то есть обладать повышенной адгезией);
- иметь такую величину теплового расширения, которая бы незначительно отличалась от расширения защищаемой конструкции;
- быть максимально недоступным для вредных факторов окружающей среды.
Также покрытие должно наноситься на всю конструкцию как можно более равномерно и сплошным слоем.
Все используемые в наши дни защитные покрытия делят на:
- металлические и неметаллические;
- органические и неорганические.
Такие покрытия, которые мы опишем далее, применяются (и весьма активно) по всему миру. Поэтому о них будет рассказано достаточно подробно.
2 Антикоррозионная защита при помощи протекторов – особенности методики
Применение протекторной защиты от коррозии трубопроводов и конструкций из металла в кислых средах не имеет смысла, что обусловлено повышенным темпом саморастворения протектора. Она рекомендуется для использования в нейтральных средах, будь то обычный грунт, речная или морская вода.
По отношению к железу более активными являются следующие металлы – магний, хром, кадмий, цинк и некоторые другие. Теоретически именно их следует применять для защиты газопровода либо другой конструкции. Но здесь имеется ряд нюансов, которые обуславливают технологическую нецелесообразность использования чистых металлов в качестве «защитников».
Магний в чистом виде, например, характеризуется повышенной скоростью собственного ржавления, на алюминии очень быстро появляется оксидная толстая пленка, а цинк без каких-либо примесей ввиду своей дендритной крупнозернистой структуры имеет свойство растворяться крайне неравномерно. Чтобы нивелировать все эти негативные явления, в чистые металлы, предназначенные для защиты трубопроводов и металлоконструкций от коррозии, добавляют легирующие компоненты. Другими словами, антикоррозионная защита, например, газопровода, подземного резервуара в большинстве случаев выполняется при помощи различных сплавов.
Часто используются сплавы на основе магния. В них вводят алюминий (от 5 до 7 процентов) и цинк (от 2 до 5 процентов), а также незначительные количества (буквально сотые либо десятые доли) никеля, свинца, меди. Защита от коррозии магниевыми сплавами применяется тогда, когда конструкция из металла (элементы трубопроводов, газопровода и так далее) функционирует в средах с показателем рН не более 10,5 (обычный грунт, водоемы с пресной или слабосоленой водой).
Такое ограничение связано с тем, что магний сначала очень быстро растворяется, а затем на его поверхности формируются соединения, характеризуемые затрудненным растворением. Стоит сказать отдельно об опасности использования магниевых композиций для защиты от коррозии – они могут стать причиной растрескивания изделий из металла, а также их охрупчивания (водородного).
Для металлоконструкций, установленных в соленой воде, газопровода, проложенного по морскому дну, рекомендуется использование протекторов на базе цинка, которые содержат:
- кадмий (от 0,025 до 0,15 %);
- алюминий (не более 0,5 %);
- медь, свинец, железо (от 0,001 до 0,005 % в сумме).
Протекторная защита трубопроводов в морской воде цинковыми составами будет гарантированно эффективной и длительной. Если же такие протекторы применять в грунте или пресных водоемах, они практически мгновенно покрываются гидроксидами и оксидами, что сводит на нет все антикоррозионные мероприятия.
А вот в соленой проточной воде, на прибрежном морском шельфе обычно эксплуатируются алюминиевые защитники от коррозии. В них содержится таллий, кадмий, кремний, индий (суммарно до 0,02 %), магний (не более 5 %) и цинк (не более 8 %). Данный состав не дает возможности появляться на алюминии окислам. Протекторная защита из алюминиевых составов используется в тех же условиях, что и из магниевых.
Цинковые протекторы обычно применяются для антикоррозионной защиты тех металлоконструкций, для которых должна быть обеспечена максимальная пожарная и взрывобезопасность (в частности, разнообразных трубопроводов для транспортировки потенциально горючих материалов, например, газопровода). Также цинковые защитные композиции не создают при анодном растворении загрязняющих соединений. За счет этого им практически нет замены, когда речь идет о защите от коррозии трубопроводов, по которым перемещают нефть, а также нефтеналивных и грузовых судов и танкеров.
1 Суть протекторной защиты металлов от коррозии
Данная антикоррозионная защита подразумевает присоединение к предохраняемой металлической поверхности специального протектора – металла с более электроотрицательными характеристиками. При растворении под действием воздуха такой протектор начинает выполнять свою функцию, которая состоит в предохранении основного изделия от разрушения.
По сути, протекторная защита трубопроводов и иных магистралей от коррозии является одним из видов катодной электрохимической методики.
Описываемый способ антикоррозионной обработки оптимален для ситуаций, когда у предприятия нет возможности возвести специальные электрические линии для организации эффективной катодной защиты от электрохимической коррозии либо их строительство признается экономически нецелесообразным. Протектор полностью выполняет свои задачи при условии, что величина переходного сопротивления между средой, окружающей обрабатываемый объект, и этим самым объектом невелика.
Сущность коррозии металлов такова, что менее активный из них при взаимодействии станет присоединять к своим ионам электроны более активного, которые будут производиться активным компонентом системы. В результате происходит сразу два одновременных процесса:
- восстановление менее активного металла (он является катодом);
- окисление менее активного металла-анода, благодаря чему и происходит антикоррозионная защита газопровода, иной магистральной сети, какой-либо металлоконструкции.
Через определенное время действие протектора заканчивается (из-за утраты контакта с предохраняемым металлом либо при полном растворении «защитника»), после чего потребуется выполнить его замену.
Как отчистить ржавчину с кузова автомобиля
Рыжие пятна, появляющиеся на металлических деталях машины, убирать следует как можно быстрее. Большинству автолюбителей известно, что при наличии на кузове автомобиля ржавчины его стоимость снижается примерно в 2-3 раза. Замена же изъеденных коррозией деталей обходится очень дорого.
Способов очистки кузова автомобиля существует несколько. Чаще всего с этой целью приобретается сильное концентрированное жидкое средство для удаления ржавчины с металла.
Иногда поврежденные места кузова обрабатывают и посредством разбавленной ортофосфорной кислоты. Еще одним неплохим способом избавления от рыжих пятен на авто считается использование смеси на основе солей цинка. В этом случае применяется электрохимический способ очистки, но, конечно же, без использования емкости. Смесь просто наносится на тряпку, намотанную на электрод. Далее последний подключается к аккумулятору.
Применение жидкой резины для гидроизоляционных работ
Виды коррозии металлов
Учитывая сложность процесса и его многообразие, классификация видов коррозии ведется по нескольким группам признаков:
- механизм – химический или электрохимический;
- окружающая среда. Выделяют общую газовую, атмосферную (с наиболее активным действием кислорода), электролитную и неэлектролитную, подземную (иначе почвенную), биологическую среды. Также агрессивной средой считаются блуждающие токи;
- условия протекания. С погружением, без погружения и частичным погружением в среду, с непосредственным контактом, через щель, в результате трения. Выделяют межкристаллитное воздействие (по границам кристаллов и зон), коррозию под постоянным или переменным электрическим напряжением;
- степень разрушения объекта. Коррозия может быть сплошной, захватывающей всю поверхность объекта (равномерной, неравномерной, избирательной) или локальной. В этом случае отмечают пятна, язвы, точки и сквозные поражения, а также межкристаллитный вариант.
Несколько примеров для лучшего понимания сути и разновидностей коррозии.
-
Повреждение днища автомобиля. Считается химическим, с активным действием влаги и атмосферного кислорода, активных газов выхлопа, дорожной «химии» и частично моющих средств при помывке авто. В случае пробоя электропроводки на днище могут воздействовать слабые токи, в этом случае коррозия будет уже электрохимической и заметно ускорится.
-
Ржавление гвоздей и другого крепежа из сплавов железа в строительных конструкциях. Химический процесс, связан с атмосферной влагой и кислородом. При повышенной кислотности материала, в котором установлен крепеж, или увеличении кислотности атмосферных осадков и газовой среды ржавление усиливается и проходит быстрее.
-
Сваи в морской воде. Активное воздействие агрессивного электролита (которым является морская вода) приводит к быстрому разрушению металлических конструкций. Скорость коррозии усиливают перепады температуры и механическое воздействие волн.
-
Поверхностное разрушение сантехнических устройств и радиаторов отопления. Это характерный пример электрохимической коррозии, где в роли электролита выступает водопроводная вода (теплоноситель в отопительной системе) и моющие средства для сантехники.
Последний вариант (на фото) – это именно коррозия, но не ржавление, поскольку сплав, как правило, создается не на основе железа.
Оцинковка кузова
Оцинковку кузова выполняет завод-изготовитель. Как правило, кузовные элементы будущей машины погружаются в емкость с расплавленным цинком. Толщина металла, который осядет на поверхности, не больше 2 мкм. Здесь действует принцип, основанный на электрохимических процессах, а именно цинк отбирает окислительные процессы на себя.
Вообще, оцинковка может выполняться тремя способами:
- Термический, о котором говорилось выше.
- Гальванический способ. Деталь погружают в электролит и цинк налипает на деталь.
- Холодный способ. Деталь окрашивают цинкосодержащим составом.
Цинковое покрытие имеет один недостаток – все дело в микропорах, которые есть в цинке.
Защита машины – процесс обязательный и автовладелец должен это понимать. Все перечисленные способы хороши и действенны, но катодный способ все же намного лучше остальных.
Происхождение термина «Холодное цинкование»
В статье «Надежные российские покрытия для промышленных объектов» компании ВМП, г. Екатеринбург (Журнал «Промышленная окраска» №05-06), указана следующая информация:
«Покрытие ЦИНОЛ, содержащее 96% (мас.) цинка имеет измеренный потенциал близкий к величинам характерным для горячего цинкования. Он незначительно меняется в течение длительного времени и способствует эффективной катодной защите. Когда данный факт был установлен впервые, покрытие ЦИНОЛ по аналогии с горячим цинкованием (т.е. покрытием, полученным погружением в расплав цинка) наименовали «холодным», термин прижился на рынке и позже был распространен на другие цинкнаполненные покрытия, наносимые лакокрасочными методами».
Эксплуатация протекторных цинкнаполненных грунтовок
Известно, что по мере окисления цинка с образованием в микропорах и на поверхности покрытия плотных продуктов химической реакции, протекторная защита постепенно снижается, а барьерная возрастает. Соотношение двух механизмов защиты и характер их изменения во времени индивидуален для каждого материала. Изначально протекторные свойства покрытия сильно зависят от содержания цинкового порошка, его размера, характера упаковки, природы пленкообразующего вещества. Чем больше содержание цинка и выше электропроводность покрытия, тем лучше они выражены. Но менее выраженные протекторные свойства цинкнаполненных покрытий могут быть компенсированы более выраженными барьерными механизмами защиты.
Защитные покрытия, применяемые в быту.
Как уже упоминалось ранее, антикоррозионной защиты требуют и обычные металлические изделия, окружающие нас в повседневном быту. В каждой квартире, а тем более в частном доме, имеется большое количество металлических деталей – балконные ограждения, заборы, решетки, гаражи, садовая техника, радиаторы, трубы холодной и горячей воды, садовые скамейки, которые покрываются со временем ржавчиной.
Доступным способом их защиты является нанесение вручную антикоррозионного покрытия в виде грунтовки или краски по ржавчине. Эти покрытия имеют специальный состав, содержащий ингибиторы и различные добавки, что позволяет наносить их непосредственно на слой ржавчины, предварительно не зачищая металл.
В состав грунтовки, например, входит преобразователь ржавчины и антикоррозионный грунт. Это очень эффективное средство, которое часто используют как самостоятельное покрытие. Такой грунт надежно будет защищать покрытую поверхность от различных атмосферных проявлений (град, снег, дождь, солнце).
Антикоррозионная краска отличается от грунта тем, что в ее состав дополнительно включен такой компонент как износостойкая эмаль, что обеспечивает очень быстрое высыхание краски на воздухе. Ее достоинство в том, что она наносится на любую поверхность (с остатками предыдущей краски, покрытую ржавчиной) из стали, чугуна, железа или железобетона. Нанесение слоя такой краски продлевает, как минимум вдвое, срок службы металлических изделий.
Из всего вышесказанного видно, что существует много различных способов, чем покрыть металл от коррозии. И в зависимости от вида покрываемого металла не составит труда выбрать нужный и эффективный, который защитит металл от ржавчины.
Дополнительная информация: Защита от ржавчины на металле в домашних условиях
Антикоррозийная защита материала в домашних условиях подразумевает применение ЛКМ-покрытий и химических средств. Свойства защитного плана обеспечивают сочетанием разных элементов: смол на основе силикона, ингибиторов, полимеров, металлической стружки и пудры.
Коррозия представляет собой процесс, сопровождающийся разрушением поверхностных слоев конструкций из стали и чугуна, возникающий в результате электрохимического и химического воздействия. Негативным следствием этого становится серьезная порча металла, его разъедание, что не позволяет использовать его по назначению.
В каждом доме, среди домашней утвари, предметов интерьера имеются материалы, инструменты или детали, сделанные из металла. Они практичны, износостойки, но рано или поздно подвергаются коррозии. Как предотвратить этот процесс?
Чем обработать металл, чтобы он не ржавел?
Пленки образуются из лакокрасочных материалов, пластмассы и смолы. Лакокрасочные покрытия недороги и удобны в нанесении. Ими покрывают изделие в несколько слоев.
Термическое воронение стали в домашних условиях? Под краску наносят слой грунта, улучшающего сцепление с поверхностью и позволяющего экономить более дорогую краску. Служат такие покрытия от 5 до 10 лет.
В качестве грунта иногда применяют смесь фосфатов марганца и железа.
Следы легкого окисления, неглубокий налет коррозии, воронение и пр. следы химического окрашивания металла (намеренноно и непреднамеренного) легко и бысто удаляет автополироль. Берите наименее абразивную и не жадничайте – импортную (США, германия и пр.) Небольшой баночки (например, на основе масла Карнаубы) хватит на очень продолжительное время, а если есть машина то остатки тем более не пропадут. (Александр Марьянко)
Коррозионное разрушение – это явление, которое видел каждый. Чем быстро снять краску с дерева в домашних условиях? Образование ржавчины на металлической поверхности лишь один из признаков.
Коррозионный процесс вызывает разъедание материала под воздействием факторов окружающей среды. Как правило, речь идет о влаге. Вода окисляет металл, провоцируя его последующее разрушение.
Не, просто воронение слабо защищает от ржавчины. Консервационная смазка, оружейная – это да.Из практического опыта – у меня воздушка (несмазанная, ну так получилось, вовремя не законсервировал) провалялась в гараже месяца 2 без дела, и за это время вороненый ствол успел покрыться мелкими “цяточками” ржавчины. Так что смазка – обязательно!